益生菌凝胶:守护肌肤微生态,打造健康美丽新境界!

在繁忙的现代生活中,肌肤问题日益成为我们关注的焦点。广州同祥堂药业有限公司深知肌肤健康的重要性,特别推出了一款益生菌凝胶产品,旨在守护您的肌肤微生态,有效平衡肌肤菌群,让您的肌肤焕发健康美丽新光彩! 益生菌凝胶以其独特的配方和功效,在护肤品市场中脱颖而出。它含有丰富的益生菌成分,能够深入肌肤底层,为肌肤注入源源不断的活力。这些益生菌与肌肤表面的菌群相互作用,共同维护肌肤的微生态平衡,有效预防肌肤问题的发生。同时,益生菌凝胶还富含多种保湿成分,能够持续滋润肌肤,让肌肤水嫩有光泽。 广州同祥堂药业有限公司在研发益生菌凝胶时,始终坚持以科学为依据,注重产品的安全性和有效性。我们严格筛选原料,确保产品的纯净度和品质。在生产过程中,我们采用先进的生产工艺和设备,确保每一瓶益生菌凝胶都能达到高的质量标准。此外,我们还拥有专业的研发团队,不断对产品进行升级和优化,以满足消费者日益增长的需求。 为了让更多消费者了解和体验到益生菌凝胶的神奇功效,广州同祥堂药业有限公司积极开展线上线下推广活动。我们不仅在各大电商平台开设官方旗舰店,还与多家实体店合作,为消费者提供便捷的购买渠道。同时,我们还定期举办优惠活动,让消费者以更实惠的价格购买到好品质的益生菌凝胶。 广州同祥堂药业有限公司始终秉承“以质取胜,诚信为本”的经营理念,致力于为消费者提供安全、有效的护肤品。我们相信,通过我们的努力,益生菌凝胶将成为越来越多消费者守护肌肤微生态、焕发健康美丽新光彩的得力助手。在未来的发展中,我们将继续不断创新,为消费者带来更多品质、高效的护肤产品。 让我们一起关注肌肤健康,选择益生菌凝胶,让广州同祥堂药业有限公司陪伴您走向美丽人生!
重要变化!国家局发布《保健食品原料目录(2023年版)》新增DHA藻油、大豆分离蛋白、乳清蛋白
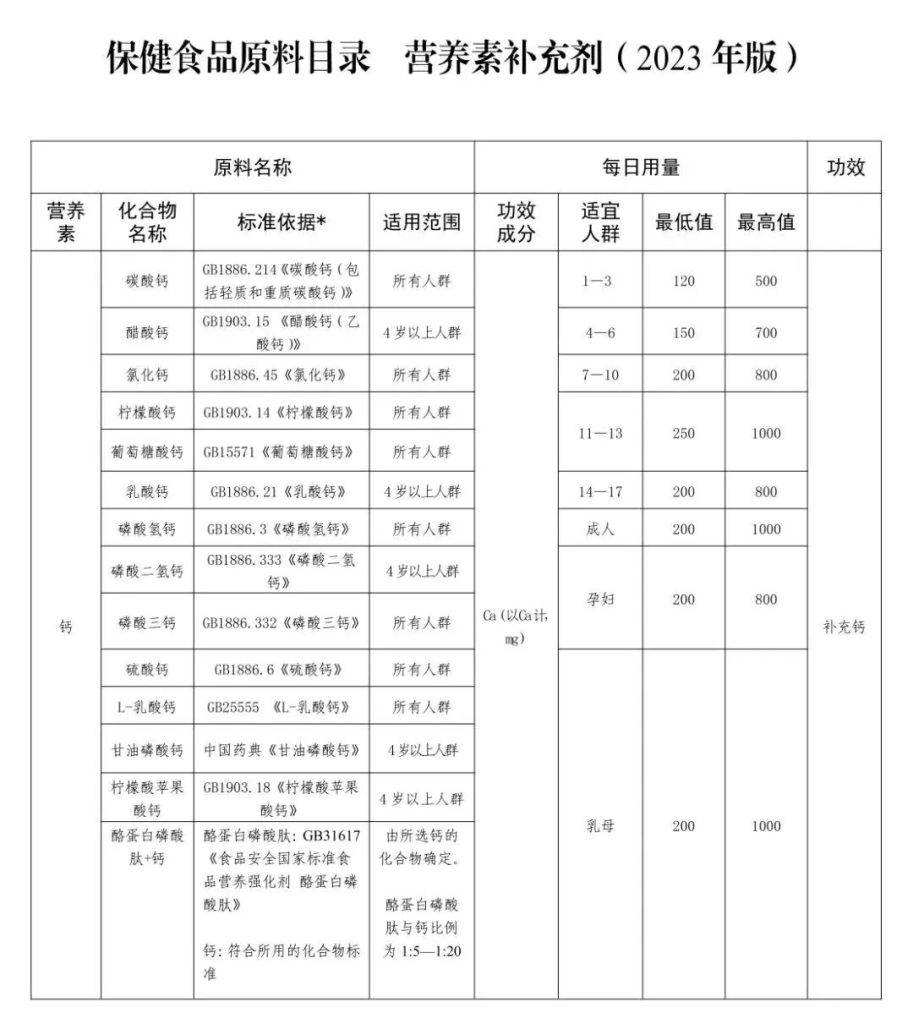
根据《中华人民共和国食品安全法》《保健食品原料目录与保健功能目录管理办法》等规定,市场监管总局会同国家卫生健康委、国家中医药局调整了《保健食品原料目录 营养素补充剂(2023年版)》《允许保健食品声称的保健功能目录 营养素补充剂(2023年版)》,制定了《保健食品原料目录 大豆分离蛋白》《保健食品原料目录 乳清蛋白》,现予公告,自2023年10月1日起施行。此前发布有关目录与本版本不一致的,以本版本为准。 附件1:《保健食品原料目录 营养素补充剂(2023年版)》 附件2:《允许保健食品声称的保健功能目录 营养素补充剂(2023年版)》 附件3:《保健食品原料目录 大豆分离蛋白》 附件4:《保健食品原料目录 乳清蛋白》
药品、医疗器械……不得以盲盒形式销售!

近日市场监管总局印发 《盲盒经营行为规范指引(试行)》 (以下简称《指引》) 为盲盒经营划出红线 推动盲盒经营者加强合规治理 《指引》中提到,药品、医疗器械、有毒有害物品、易燃易爆物品、活体动物等在使用条件、存储运输、检验检疫等方面有严格要求的商品,不得以盲盒形式销售。食品、化妆品,不具备保障质量安全和消费者权益条件的,不应当以盲盒形式销售。 近年来盲盒相关产品受到不少年轻消费者青睐 引发社会广泛关注 与此同时 盲盒经营过程中的 信息不透明、虚假宣传、 “三无”产品、售后服务不到位等问题 也逐渐凸显 为规范盲盒经营行为,维护公平竞争的市场秩序,保护消费者合法权益,维护社会公共利益,《指引》具体从四个方面予以规范: 制定负面销售清单 对于不适宜进入盲盒领域的药品、医疗器械、活体动物、易燃易爆物品等,提出不得以盲盒形式销售;对于关系人民群众健康的化妆品、食品,作出限定性表述。 明确信息披露范围 要求盲盒经营者将盲盒内物品的商品价值、抽取规则、抽取概率等关键信息以显著方式对外公示,保证消费者在购买前知晓真实情况。 鼓励建立保底制度 鼓励盲盒经营者通过设定抽取时间、抽取金额上限和次数上限等方式引导理性消费,自觉承诺不囤货、不炒作、不直接进入二级市场。 完善未成年人保护机制 对盲盒销售对象的年龄作严格限制,要求不得向未满8周岁未成年人销售。要求盲盒经营者采取有效措施防止未成年人沉迷,保护未成年人身心健康。鼓励地方有关部门出台保护性措施,推动净化学校周边消费环境。
2023年医疗器械法规标准汇总

近日,广东器械审评整理了2023年版本医疗器械法规汇总(2023年2月1日更新),内容如下: 一、行政法规 序号 法规 1 医疗器械监督管理条例(国务院令第739号) 二、部门规章 序号 法规 1 《医疗器械注册与备案管理办法》(国家市场监督管理总局令 第47号) 2 《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令 第48号) 3 《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局令 第6号) 4 《医疗器械生产监督管理办法》(国家市场监督管理总局令第53号) 5 《医疗器械经营监督管理办法》(国家市场监督管理总局令第54号) 6 《药品医疗器械飞行检查办法》(国家食品药品监督管理总局令第14号) 7 《医疗器械使用质量监督管理办法》(国家食品药品监督管理总局令第18号) 8 《医疗器械通用名称命名规则》(国家食品药品监督管理总局令第19号) 9 国家药监局 国家卫生健康委关于发布《医疗器械临床试验质量管理规范》的公告(2022年第28号) 10 《医疗器械召回管理办法》(国家食品药品监督管理总局令第29号) 11 《国家食品药品监督管理总局关于调整部分医疗器械行政审批事项审批程序的决定》(国家食品药品监督管理总局令第32号) 12 《医疗器械标准管理办法》(国家食品药品监督管理总局令第33号) 13 《医疗器械网络销售监督管理办法》(国家食品药品监督管理总局令第38号) 14 《医疗器械不良事件监测和再评价管理办法》(国家市场监督管理总局令第1号+A14:B28) 三、工作文件 1、临床试验篇 序号 法规 1 国家药监局关于实施《医疗器械临床试验质量管理规范》有关事项的通告(2022年第21号) 2 关于发布医疗器械临床试验设计指导原则的通告(2018年 第6号) 3 关于发布接受医疗器械境外临床试验数据技术指导原则的通告(2018年 第13号) 4 国家药监局关于发布需进行临床试验审批的第三类医疗器械目录(2020年修订版)的通告(2020年第61号) 5 […]
学术论文-妇因美医用敷料妇君康(洗剂)联合氟康唑胶囊治疗霉菌性阴道炎的临床观察
联合氟康唑胶囊治疗霉菌性阴道炎的临床观察-760x1024.png.webp)
学术推广-中药熏洗联合妇因美卡波姆宫颈凝胶治老年性阴道炎疗效观察

学术论文-微波联合卡波姆凝胶治中重度宫颈糜烂的疗效观察

学术论文-思韵美多种维生素锌硒片对免疫性不孕不育患者临床效果

学术论文-卡波姆凝胶医治慢性宫颈炎的40例临床观察









